新葡的京集团8814分子酶学工程教育部重点实验室李全顺教授团队,针对类风湿性关节炎的关键信号分子miR-23b,构建氟化修饰型树枝状高分子作为基因递送载体,实现miR-23b在关节炎动物模型中的稳定递送,取得了良好的治疗效果;同时,研究揭示了miR-23b能够抑制TAB2、TAB3以及IKK-α表达,阻断NF-κB炎症信号通路,并诱导巨噬细胞凋亡,实现体内抗炎功能。研究结果以Fluorinated polyamidoamine dendrimer-mediated miR-23b delivery for the treatment of experimental rheumatoid arthritis in rats为题,于2023年2月20日在学术期刊《Nature Communications》正式发表。论文第一完成单位为新葡的京集团8814,新葡的京集团8814韩浩博博士(鼎新学者)为该论文的第一作者,新葡的京集团8814李全顺教授为该论文的通讯作者。

类风湿性关节炎是一种自身免疫介导的慢性炎症疾病,以进行性关节滑膜炎症及骨侵蚀为主要病理特征。在调控滑膜巨噬细胞的炎症信号网络中,寡核苷酸分子miR-23b具有显著的抗炎效果,因此有潜力成为新的药物开发靶点。为提高小核酸miR-23b的稳定性及治疗效果,本研究以树枝状高分子聚酰胺-胺为母体,通过氟化修饰手段,构建了聚酰胺-胺高分子衍生物FP为基因递送载体。FP与miR-23b通过静电组装,形成稳定的纳米复合物,胞内递送后通过靶向TAB2/3及IKK-α基因,抑制NF-κB信号通路激活,降低胞内炎症因子释放,诱导细胞凋亡,实现抗炎生物学功能(图1)。
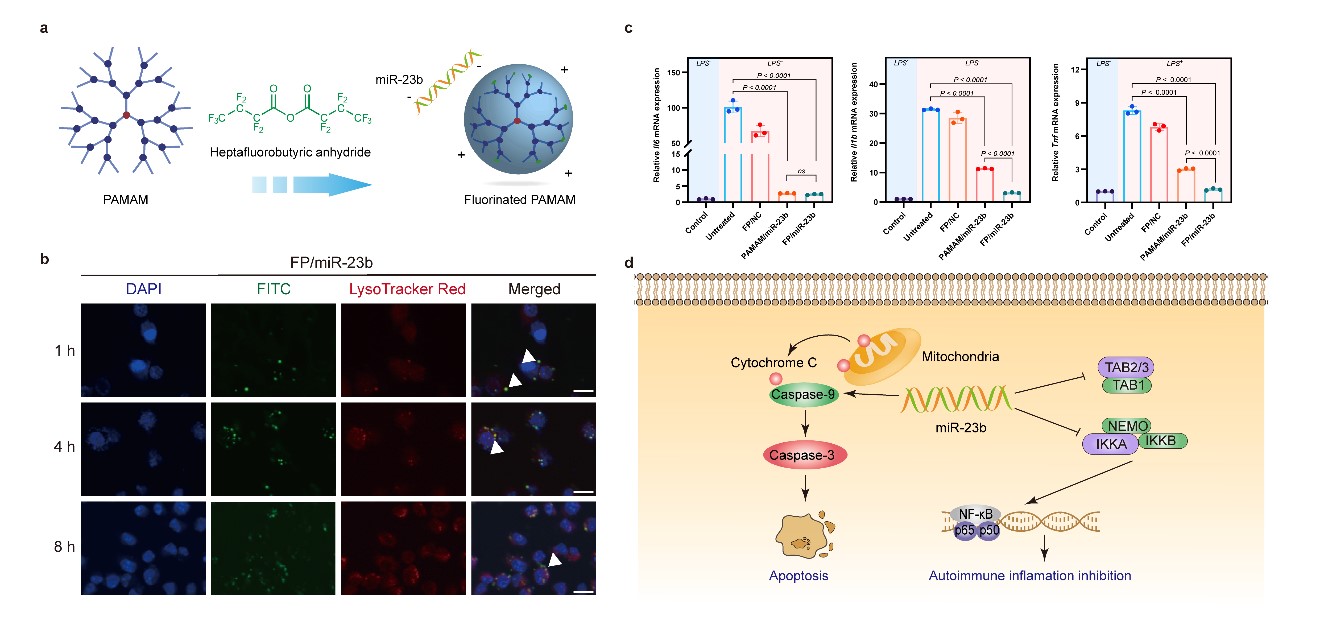
图1 FP/miR-23b纳米复合物诱导细胞凋亡及胞内炎症反应
将纳米复合物通过尾静脉注射到类风湿性关节炎动物模型后,纳米复合物能蓄积在受损关节组织处,提高滑膜组织处miR-23b表达含量,诱导滑膜细胞发生凋亡及抑制炎症反应,有效缓解关节炎动物关节处肿胀、促炎因子分泌以及关节骨组织损伤等病理现象,体现良好的治疗效果(图2),同时并未引起肝肾功能损伤,具有良好的生物相容性。本研究不仅有助于深入理解类风湿性关节炎发病机制,并针对疾病关键靶点开发新的基因治疗策略,同时为基于寡核苷酸分子的其他自身免疫疾病精准治疗提供了新的思路。
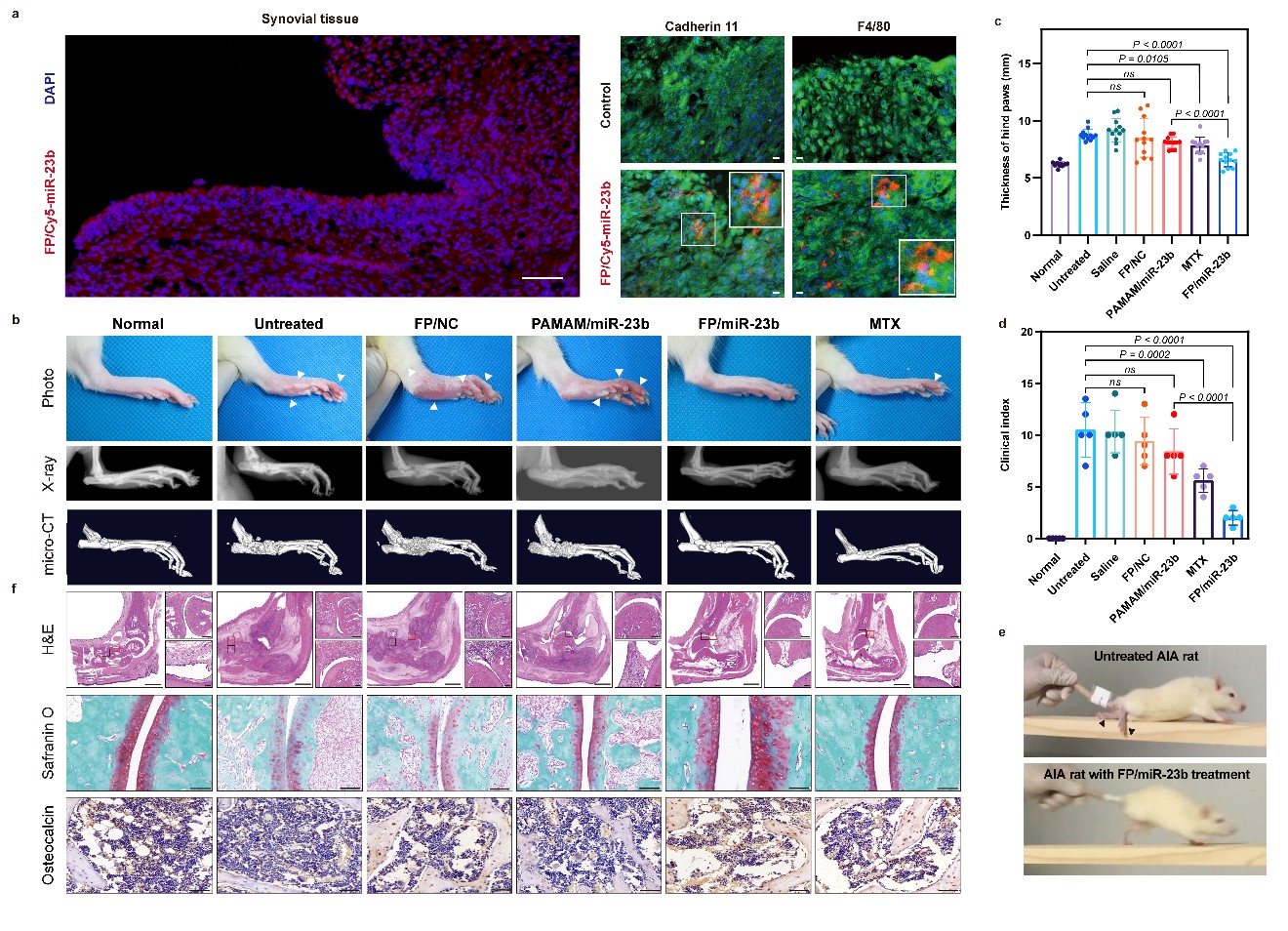
图2 FP/miR-23b纳米复合物治疗类风湿性关节炎大鼠模型
该研究工作得到了国家重点研发计划(2018YFC1105401)、国家自然科学基金(81872928、320171267、32000897)、吉林省教育厅科学技术研究项目(JJKH20211054KJ)的资助。
论文信息:Haobo Han,Jiakai Xing, Wenqi Chen, Jiaxin Jia, Quanshun Li*. Nat. Commun. 2023, 14, 944.
全文链接:https://www.nature.com/articles/s41467-023-36625-7.