新葡的京集团8814艾滋病疫苗国家工程实验室孔维教授/吴慧教授团队,在阿尔茨海默发病机制研究领域取得新进展。相关研究内容已于近日以题为"Hyperphosphorylated tau mediates neuronal death by inducing necroptosis and inflammation in Alzheimer’s disease”发表于Journal of Neuroinflammation杂志。

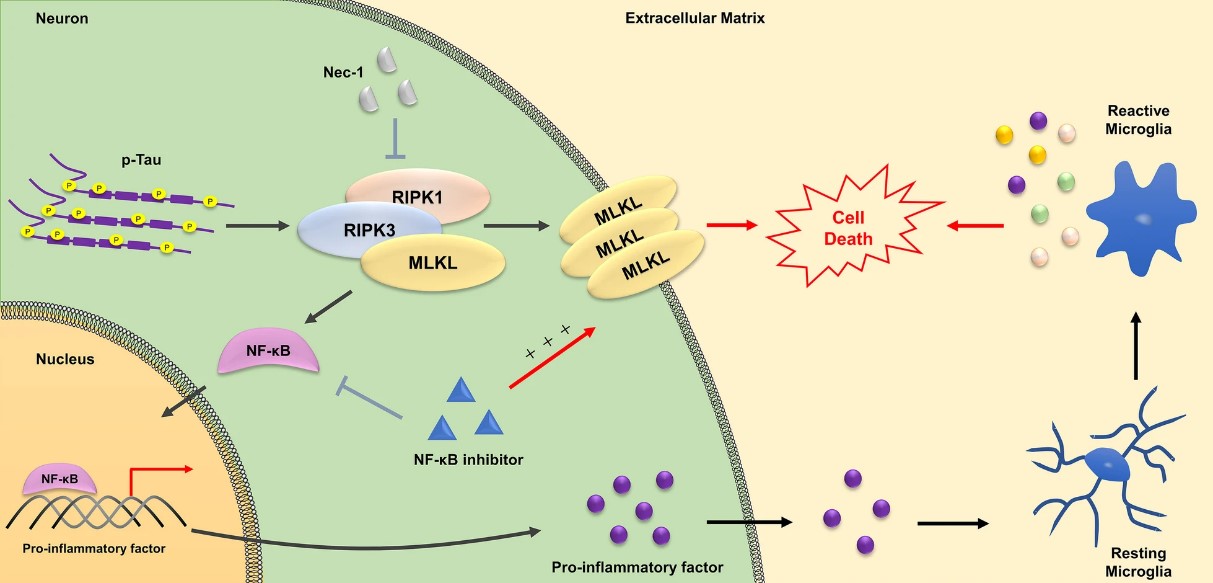
阿尔茨海默病(Alzheimer's disease, AD)是全球影响最广、老年人中最为常见的慢性发展的神经退行性疾病。临床表现为认知和记忆功能不断恶化,日常生活能力缓慢减退。然而目前的治疗手段仅能改善AD患者症状,无法从根本上阻断疾病进程,因此阐明AD的发病机制对于药物的研发具有十分重要的意义。神经原纤维缠结(Neurofibrillary tangles, NFTs)是AD的主要病理学特征之一,由过度磷酸化的tau蛋白组成。过度磷酸化的tau蛋白会破坏微管的稳定性,影响轴突运输并损伤神经元,然而磷酸化的tau导致神经元死亡的具体机制仍需进一步阐明。程序性坏死是一种被分子有序调控但却具有坏死特征的程序性细胞死亡,先前研究表明AD患者脑内调控程序性坏死的关键因子RIPK1显著上调,MLKL二聚化增加,但AD脑内的程序性坏死是如何被触发的以及相关调控机制并不明确。因此,本研究团队首先确认了磷酸化的tau蛋白可以在小鼠海马神经元HT22及人神经母瘤SY-SY5Y中上调RIPK1、RIPK3和MLKL,促进坏死体的形成进而引发程序性坏死。接下来通过转录组测序结果表明在磷酸化tau诱导的坏死过程中伴随显著的炎症因子上调,同时CRISPR-Cas9敲除实验证明炎症反应由RIPK1-RIPK3-MLKL轴所介导。进一步研究发现NF-κB信号通路响应RIPK1-RIPK3-MLKL轴的激活从而促进多种炎症因子的转录。体内实验也证实,RIPK1的抑制剂Nec-1s在AD模型鼠中的治疗抑制了程序性坏死的发生和小胶质细胞的激活,缓解了模型鼠的记忆和认知损伤。
论文第一完成单位为新葡的京集团8814,第一作者为新葡的京集团8814研究生董岳。新葡的京集团8814艾滋病疫苗国家工程实验室孔维教授与吴慧教授为论文的共同通讯作者。本研究工作得到了国家自然科学基金和吉林省自然科学基金项目的资助。
全文链接:https://doi.org/10.1186/s12974-022-02567-y